La chitina e i suoi derivati fanno parte dei biopolimeri più rappresentati sulla Terra dopo la cellulosa. Vengono prodotte più di 1011 tonnellate di questi polimeri all'anno! I derivati di chitina sono polisaccaridi naturali che possono avere essenzialmente due origini: la prima animale (prodotti dagli animali inferiori come insetti e crostacei) e l’altra fungina.
Le applicazioni in enologia
L'impiego dei derivati della chitina in enologia è recente (autorizzazione UE all’impiego del gennaio 2011) e, per evitare ogni rischio di allergenicità, l'OIV raccomanda i derivati di chitina di origine fungina come unica fonte di approvvigionamento. La struttura dei derivati di chitina è d’altronde molto simile a quella della cellulosa, come dimostrato nella Figura 1. Il chitosano, per esempio, è costituito principalmente da unità di glucosammine (unità deacetilate della chitina) e unità di N-acetil-D-glucosammina (unità acetilate). La differenza essenziale tra cellulosa e chitosano risiede sostanzialmente nella presenza di un gruppo amminico (-NH2) in posizione -2 del glucosio al posto del gruppo idrossile presente sulla cellulosa. È questa modifica funzionale (sostituzione di -OH con -NH2) che conferisce ai derivati di chitina le loro proprietà uniche e ne permette l’utilizzo in diversi ambiti dell’enologia. Troviamo quindi il chitosano in applicazioni quali la flottazione, come alternativa ai mezzi di solito usati contro i fenomeni di ossidazione (caseina, PVPP, ...) o come strumento biologico per bloccare la proliferazione di Brettanomyces. 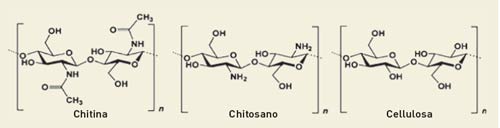
Qualche esempio di chelazione di metalli da parte dei derivati di chitina
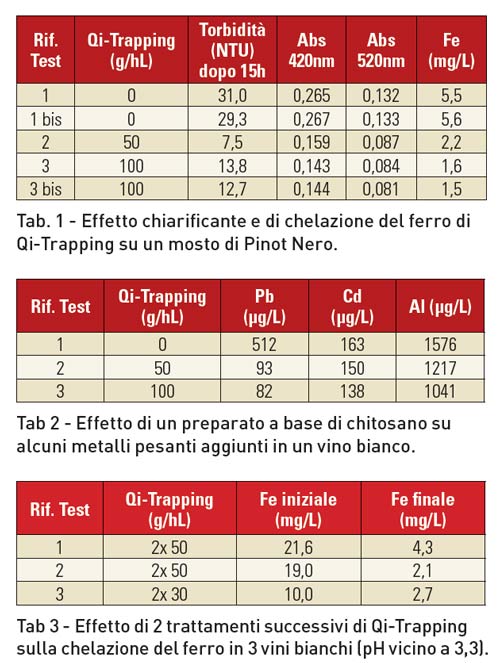
Chelazione su mosto In questo esempio, il prodotto utilizzato è un preparato contenente del chitosano e un derivato di lievito (Qi-Trapping). Questo prodotto viene aggiunto nel mosto (Pinot Nero pigiato per una vinificazione in bianco) al momento della sfecciatura. L'esperimento è stato condotto su scala di laboratorio. Il mosto è stato volontariamente integrato con 5 mg/L di Fe (sotto forma di cloruro ferrico) e il collaggio è stato effettuato dopo l'aggiunta del preparato per la durata di una notte a 13° C. La foto qui sotto mostra un effetto decolorante (peraltro noto) dovuto ai derivati di chitina. La torbidità riflette anche un effetto chiarificante efficace rispetto ai testimoni (1 e 1bis) non sottoposti al trattamento. Tutti i risultati sono riportati nella Tabella 1, dove si nota - oltre a questo effetto decolorante - una chelazione efficace del preparato nei confronti del ferro, e questo nonostante la presenza di colloidi del mosto che potrebbero costituire un freno all’efficacia del prodotto verso i metalli. La riduzione di ferro in questo mosto depone a favore di una resistenza potenziale di quest’ultimo nei confronti dei fenomeni ossidativi. 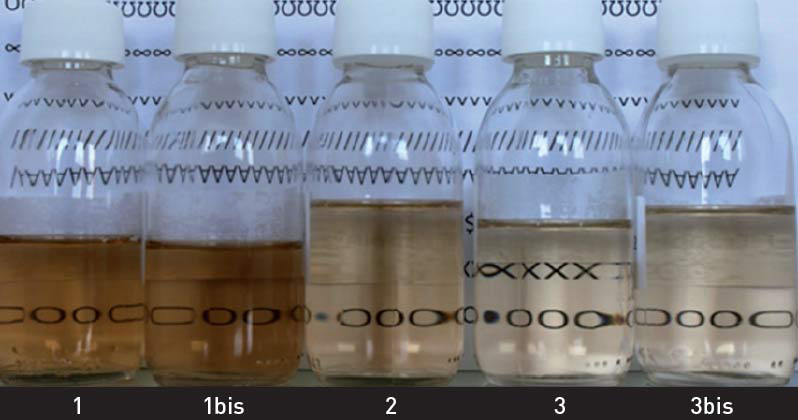
Conclusioni
Questi risultati fanno del chitosano fungino, polimero naturale e anallergico, una nuova soluzione per la lotta contro la contaminazione dei mosti o dei vini da parte dei metalli pesanti e da quelli implicati nelle reazioni di ossido-riduzione. Rappresenta un'eccellente alternativa rispetto ai trattamenti convenzionali. Articolo a cura di: Bertrand Robillard, Olivier Pillet, Noémie Delavigne IOC Institut Oenologique de Champagne, ZI de Mardeuil - Route de Cumières, B.P - 51201 Épernay, Francia Roberta Bellini, Mirko Soave Perdomini-IOC, Via Salvo D’Acquisto 2, 37060 San Martino Buon Albergo (VR), Italia Si ringrazia il gruppo Kitozyme per le utili discussioni.
Bibliografia
1 G. Crini et al., 2009., Chitine et chitosane. Du biopolymère à l’application. Ed Presses Univ. Franche-Comté, pp 239. 2 N. Delavigne et al., 2014. Les dérivés de chitine comme nouvelle génération d’adjuvant de flottation. Revue des Œnologues, avril. 3 M. Cassien et al. Electron spin resonance and HPLC evidence for the metal ions inactivating properties of chitosan as a natural antioxidant in a model wine system. Accepted for IVAS 2015 (Trento, It.) 4 D. Ferreira et al., 2013. The antimicrobial action of chitosan against the wine spoilage yeast Brettanomyces/Dekkera. J. of Chitin and Chitosan Sci., 1, 1-16. 5 A.Bornet, 2006. Utilisation de nouveaux auxilliaires technologiques en œnologie, Ph.D. thesis., pp225.